Spécialiste des modèles de cancers gastriques et des cellules souches cancéreuses, l’équipe de Christine Varon (BRIC) s’est associée à celle de Majid Khatib (BRIC) afin de mieux appréhender l’implication des convertases dans les cancers gastriques de type diffus et les cancers gastriques de type intestinaux.
« Majid Khatib et Christine Varon se demandaient si le blocage des convertases pouvait bloquer les propriétés nocives des cellules souches cancéreuses » introduit Anissa Zaafour, doctorante.
Afin de répondre à cette question, l’étudiante a procédé à une analyse bio-informatique des bases de données de cancer en ligne et a montré que plusieurs de ces convertases – dont la furine – sont des marqueurs de très mauvais pronostic dans le cancer gastrique.
« Nos travaux avaient donc pour objectif de découvrir si le ciblage de ces enzymes pouvait bloquer les propriétés tumorigéniques et invasives des cellules souches cancéreuses » détaille la doctorante.
Anissa Zaafour a alors testé un inhibiteur pharmacologique des convertases sur des organoïdes tumoraux de cellules souches. Dans ces conditions spécifiques, moins de cellules souches se sont développées après traitement et celles restantes étaient moins agressives.
« Ce test nous a permis d’observer un impact significatif sur la tumorigénicité des cellules souches sur 4 lignées cellulaires de cancer gastrique que nous avons testées. »
« Un autre test mis en place par notre équipe il y a quelques années permet de mesurer la capacité des cellules souches à faire ressortir les drogues de chimiothérapie grâce à un colorant fluorescent. Ce mécanisme est impliquée dans la résistance aux traitements. Ici, la drogue ciblant les convertases bloque ce mécanisme d’efflux » ajoute Christine Varon.
Les scientifiques ont ainsi identifié des mécanismes moléculaires par lesquels passent les proprotéines convertases dans les cellules souches cancéreuses.
Accompagnée par Coralie Genevois, directrice technique de la plateforme Vivoptic de TBMCore, Anissa Zaafour a poursuivi ses travaux in vivo lors de sa thèse.
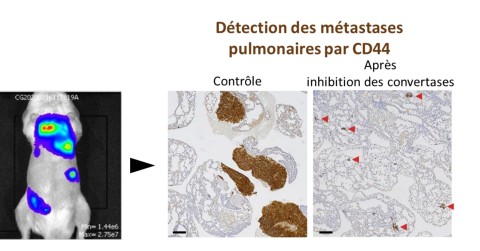
« Nous avions vu in vitro que les capacités d’invasion des cellules souches cancéreuses étaient fortement diminuées et que cela passait par des voies de signalisation d’invasion et de souchitude. Nous nous sommes demandés si ce résultat pouvait être confirmé in vivo». Pour vérifier cela, l’équipe a procédé à l’injection des cellules dans la circulation sanguine de souris immunodéficientes afin de mimer la dissémination métastatique. « Nous avons pu suivre ces cellules par bioluminescence et regarder ensuite les organes colonisés. Nous avons alors observé une diminution du pourcentage de souris porteuses de tumeurs et montré qu’elles étaient de plus petite taille. Cela confirme donc bien les tests fait in vitro » conclut Anissa Zaafour.
Ainsi, la répression des proprotéines convertases représente une nouvelle stratégie pour cibler les cellules souches cancéreuses et diminuer la propagation métastatique dans le cancer gastrique.
Afin d’aller plus loin dans ces travaux, une thèse est en cours sur le ciblage spécifique d’une de ces convertases. Ces recherches sont menées par Ana Sofia Vasquez Uriola (Equipe 4 BRIC), en collaboration avec l’équipe de Majid Khatib.
Anissa Zaafour se concentre quant à elle sur la dissémination métastatique et le mécanisme de dormance dans le cancer gastrique à l’origine des récidives.
L'équipe "Cancers digestifs associés à l’infection par Helicobacter, cellules souches cancéreuses et stratégies thérapeutiques" du BRIC